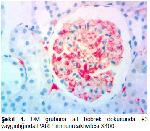
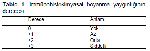Diabetes mellitus; hiperglisemi, dislipidemi, glikozüri
ve bunlara eşlik eden bir grup metabolik bozukluğu içine
alan kronik bir hastalıktır
10. Makroanjiopatik ve
mikroanjiopatik komplikasyonları olup mikroanjiopatik
komplikasyonlar; nefropati, retinopati ve nöropati olarak
gruplandırılabilir
5. Diyabetik nefropati (DN); diyabetin
geç bir bulgusu olmakla beraber, DN gelişmeden önce
fizyolojik, patolojik ve klinik belirtiler ortaya çıkmaktadır
11. Hücre içi glikoz konsantrasyonundaki aşırı artış,
glikozun heksozamin yolağına geçmesine ve sonuçta
diyabetin pek çok komplikasyonunun oluşmasına neden
olabilmektedir
6. Hiperglisemi, serbest oksijen
radikallerinin oluşum hızını artırırken, koruyucu
antioksidan sistemlerin kapasitesini düşürür. Bu durum
diyabete bağlı komplikasyonların oluşumu üzerinde etkili
olabilir
12. Böbrek tubüllerinde görülen glikojen
birikimleri, hücre ölümüne kadar gidebilen hasarların
oluşumunda etkili olabilir
13. Diabetik nefropati,
böbreğin bütün bölümlerini kapsayan yapısal
değisiklikleri içerir, fakat en karekteristik değişiklikler
glomerüllerde saptanmıştır
14. Diabetik nefropatinin
erken dönemlerinde; glomerül ve tübüllerde hipertrofi,
tübüler vakuolizasyon, glomerül ve tübül bazal
membranlarında kalınlaşma, glomerüllerde mezangial
matriks ve hücre artışı gibi histopatolojik değişikliklerin
geliştiği yapılan çalışmalar ile kanıtlanmıştır
15.
Deneysel olarak diyabet oluşturulan sıçanlarda ve
diyabet hastalarında oksijen radikallerinin ve lipid
peroksidasyonunun arttığı tespit edilmiştir
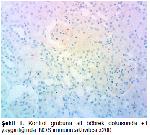
16. STZ
enjeksiyonu ile deneysel diyabet oluşturulmuş bir
çalışmada; glomeruler yumağın düzensiz bir görünüm
alması, kapillerin genişlemesi, lökosit ve eritrosit
birikimlerinin oluşumu gibi patolojilerin iNOS'un artması
neticesinde oluştuğu sonucuna varılmıştır
17.
Hücre ile peritübülar mesafe arasında iyon
taşınmasında çok fazla değişiklik olması, bazal membran
genişlemelerine; hücrede enerji için gerekli olan ATP'nin
azalması ise mitokondriyal bozulmalara neden
olmaktadır18. Böbrek tübüllerinde, özellikle proksimal
tübülde, STZ ve sitokinlerin iNOS'u artırması, böbrek
dokularındaki pek çok patolojik değişikliğin NO ile ilgili
olabileceğine işaret etmektedir13. Apoptozis sürecinde
kaspazlar önemli bir yer tutmakta ve pek çok hücrede inaktif proenzim formunda yaygın bir şekilde
bulunmaktadırlar. Ancak bir kez aktive olduklarında bir
proteaz kaskadının başlamasına izin veren diğer
prokaspazları aktive edebilirler. Bir kaspazın diğer
kaspazı aktive edebildiği bu proteolitik kaskat, apoptotik
sinyal yolaklarını uyararak hücrelerin hızlı bir şekilde
ölümüne neden olur. Kaspazlar spesifik olarak, bir
Asparajin rezidüsü icin mutlak gerekli substratlarında bir
tetrapeptid sekansını tanır ve parçalar. Efektor kaspazlar
substratların bir bölümü üzerinde etki ederek hücresel
proteinlerin proteolizisine ve apoptozis aracılığı ile
ölümüne neden olurlar. En iyi tanımlanmış olan kaspaz
substratı, DNA onarımında rol alan bir çekirdek proteini
poly-(ADP-riboz) polimeraz (PARP)'dır. PARP spesifik
kaspaz parçalanması için hedeflenmiş başlangıç
proteinlerinden biridir19. PARP, DNA tamirinden
sorumlu nükleer enzim olup aşırı aktive olursa apoptoz
ve nekroza sebep olur20. Bu mantığa dayalı olarak
yapılan bir çalışmada PARP'ın inhibe edildiği farelerde,
kontrol farelere göre septik şokun prognozunun daha iyi
seyrettiği görülmüştür. Septik şok bakteriyel
lipopolisakkaritlere bir yanıttır. Bu durumda makrofajlar
aktive olur. Birçok interlökinin eksprasyonu iNOS'u aktive
eder. Bu inflamasyon sonucu oluşan reaktif oksijen
ürünleri DNA ile reaksiyona girer. Bunun sonucunda
endotel hücrelerinin DNA sarmalları kırılır. Bu durum
PARP'in aşırı aktivitesine neden olarak, geniş
kanamalarla birlikte endotel hücrelerini ölüme götürür21.
Diyabet, dokularda serbest radikalleri ve lipid
peroksidasyonunu artırması nedeniyle hücrelerin
apoptoza gidişini patolojik düzeyde artırmaktadır16.
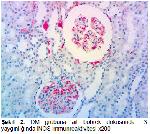
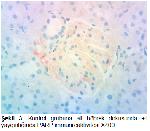
Yaptığımız çalışmada diyabetik böbrek hasarının
oluşumu ile iNOS ve PARP ekspresyonu arasında
anlamlı bir ilişki olduğu görüldü. Diyabetik böbreklerde
iNOS ve PARP immunreaktivitelerinin artmasının, SOR
ve apoptotik mekanizmalarla hasar oluşumuna sebep
olan diyabet için beklenebilir bulgular olduğu ve litaretür
bilgileri ile de tamamen uyumluluk arzettiği görüldü.
Sonuç olarak bu çalışma ile apoptoz ve hücre
sağkalımının hücresel mekanizmalarının ortaya konması
ile diyabetik nefropati gibi pek çok hastalığın tedavisinde
yeni tedavi stratejilerinin geliştirilmesine yönelik
çalışmaların güncelleştirilebileceği kanaatine varılmıştır.