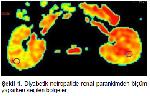
Diyabetes mellitus hiperglisemi ile karakterize bir metabolizma bozukluğudur. Dünya nüfusunun yaklaşık %1-2‟sini etkileyen ve prevalansi giderek artan sık karşılaşılan endokrin metabolik hastalıklarından biridir. Yaklaşık % 97'si Tip 2 DM'dir
11.
Diyabetes mellitusta asıl sorun uzun sürede oluşan kronik mikrovasküler ve makrovasküler komplikasyonlarıdır. Diyabetin vasküler komplikasyonları bütün dünyada en önemli morbidite ve mortalite nedeni olmayı sürdürmektedir. Bu komplikasyonlardan biri de hem Tip 1 hem de Tip 2 DM' da gelişebilen diyabetik nefropatidir. Diyabetik nefropati diyabetik olgularda morbidite ve mortalitenin en önemli nedeni olup artan sayıda hastanın son dönem böbrek yetmezliğine yakalanmasına yol açan çok önemli bir sağlık sorunudur. Diyabetik nefropati diyabetin geç bir bulgusu gibi görünmekle birlikte, DN'den önce fizyolojik, patolojik ve klinik belirtiler olur1,12.
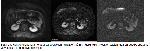
Daha hızlı ve güçlü MR cihazlarının kullanıma girmesi ile birlikte abdomende difüzyon ağırlıklı görüntüleme uygulamaları daha yaygın olarak yapılmaya başlanmıştır. Ekoplanar görüntüleme tekniğinin geliştirilmesi ile ultra hızlı görüntüleme mümkün olmuş ve sadece bir nefes tutmayla difüzyon ağırlıklı MR incelemeleri gerçekleştirilebilmektedir. Batın difüzyonla ilgili yapılan çalışmaların çoğunluğu single shot (ssEPI) tekniğiyle saniyeden daha düşük bir zaman biriminde görüntü alır ve böylece fizyolojik hareketlerden etkilenmemiş olur. Ekoplanar görüntüleme tekniğine nefes tutulmasının da eklenmesiyle solunum artefaktları ortadan kaldırılabilmekte ve batında ADC ölçümleri yapılabilmektedir13-17.
Daha önce yayımlanmış çalışmalar, nefes tutmalı difüzyon MR görüntüleri ile yapılmışken, Thoeny ve arkadaşlarının yaptığı çalışma solunum esnasında gerçekleştirilmiş ve belirgin hareket artefaktı izlenmemiştir7. Bizim çalışmamızda da solunum artefaktlarının minimalize edilebilmesi amacıyla nefes tutmalı difüzyon ağırlıklı görüntüler alındı.
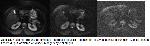
Böbreklerin DAMRG ile değerlendirildiği çalışmalarda, medulla ve renal korteksten ayrı ayrı ölçümler yapılmıştır. Cova ve arkadaşlarının yaptığı çalışmada çalışmamızda olduğu gibi korteks ve medullada ayrı ayrı ADC değerleri bulmayı denememişler, region of interest (ROI) belirtecini yaklaşık olarak kortikomeduller bileşke seviyesine yerleştirmişlerdir. Çünkü ROI' yi renal korteksin ve medullanın üzerinde ayrı ayrı ayarlamak zordur. Bu zorluk Fukuda ve arkadaşları tarafından da belirtilmiştir. Fukuda böbreklerin merkezinin perfüzyondan en az etkilendiğini belirtmiş ve değerlendirilmenin bu bölgeden yapılmasını önermiştir3,18. Biz de çalışmamızda kortikomeduller bileşkeyi içerecek şekilde geniş ROI belirteci kullandık.
Noninvaziv bir yöntem olan fonksiyonel manyetik rezonans görüntüleme teknikleri ile glomerüler filtrasyon, tübüler konsantrasyon ve transit renal kan volümü ve perfüzyon, difüzyon ve oksijenasyon değerlendirilebilmektedir. Ayrıca akut ve kronik böbrek yetmezliğinde ve renal arter darlığı olan hastalarda parankimi değerlendirmede kullanışlı bir tekniktir. Difüzyon ağırlıklı görüntülemenin önemi fonksiyonel değişimler, böbrek enfeksiyonu, hidronefroz, pyonefroz ve tümör gibi çeşitli patolojik durumlarda da ortaya konulmuştur. Yapılan çalışmalarda akut böbrek yetmezliği, kronik böbrek yetmezliği ve renal arter stenozu olan hastaların böbreklerinin ADC değerlerini normal böbreklerin ADC değerlerine kıyasla anlamlı ölçüde düşük bulunmuştur19-21.
Kronik renal yetmezliği olan hastalarda yapılan bir çalışmada normal böbreklere kıyasla ADC değerleri hem korteks hem de medullada anlamlı olarak düşük bulunmuştur22.
Yıldırım ve ark.23 renal arter stenozu olan hastaların renal ADC değerlerini sağlıklı böbreklerin ADC değerlerine kıyasla anlamlı ölçüde düşük bulmuşlardır.
Chan ve ark.9 renal pelviste saptanan ADC değerinin pyonefrotik böbrekte hidronefrotik böbreğe göre daha düşük bulmuşlardır.
Hipertansif hastalarla yapılan bir çalışmada ise renal ADC değerlerinde normal böbreklere kıyasla anlamlı fark bulunmamıştır24.
Ries ve ark.25 17 diyabetik ve 16 sağlıklı fareler üzerinde diyabetin böbrek "ADC" değerleri ile ilişkisini araştırmışlardır. Böbrek ADC değerleri olarak 0, 130, 260, 390 sn/mm² kullandıkları çalışmalarında denekleri ödematöz yaralanma olan diyabetik böbrek, atrofik hücrelerin dominant olduğu diyabetik böbrek ve nekrozun dominant olduğu diyabetik böbrek şeklinde gruplandırmışlar. Korteks, dış medullanın dış ve iç bandı, iç medulla olarak ayırdıkları tüm renal kompartımanlarda kontrol grubuna göre "ADC" değerlerinde anlamlı farklılık bulamamışlardır. Ancak, ödematöz tipte hücresel yaralanmada, dış medulla dış bandından elde olunan "ADC" değerlerinde kontrol grubuna göre anlamlı olarak düşük bulmuşlardır.
Bu çalışmada diyabetik nefropatili hastalarda b600, b1000 için ADC değerleri sağ böbrek (p=0.002, p=0.001), sol böbrek (p=0.002, p=0.001) ve ortalama böbrek (p=0.001, p=0.001) sağlıklı kontrol grubu ADC değerine göre istatistiksel olarak anlamlı bulundu. Diyabetik nefropati grubunda ortalama b100 için ADC değerleri sağ böbrek (p=0.150), sol böbrek (p=0.121) ve ortalama böbrek (p=0.128) sağlıklı kontrol grubu ADC değerine göre düşük olmakla beraber istatistiksel olarak anlamlı değildi. Yani diyabetik nefropati grubunda orta ve yüksek renal ADC değerlerinde anlamlı düşüş saptandı.
Kronik böbrek yetmezliğinde nefron kaybına bağlı olarak su hareketliliğindeki azalmaya, renal arter stenozunda ise renal iskemi ve korteks perfüzyonundaki azalmaya ve intraselüler ödeme bağlı renal parankimal ADC değerlerinin azaldığı düşünülmektedir. Çalışmamızda tespit ettiğimiz renal ADC değerlerindeki düşüşün diyabetik nefropati grubunda gelişen difüz glomeruloskleroza, sekonder ekstravasküler ekstraselüler bölgedeki suyun serbest difüzyonu kısıtlanmasına ve renal iskemiye bağlı olduğunu düşünmekteyiz.
Çalışmamızda grupların kendi içinde sağ ve sol böbrekleri karşılaştırıldığında ortalama ADC değerleri arasında anlamlı fark saptanmadı. Grup 1'deki tip 1 ve tip 2 diyabetik nefropatili hastalar b100, b600 ve b1000 ADC değerleri açısından karşılaştırıldığında aralarında istatistiksel olarak anlamlı fark bulunamadı. Bu iki bulgumuz her ne kadar tip1 DM ve tip 2 DM hastalarında diyabetik nefropati gelişim mekanizmaları aynı olmasa da gelişen nefropatide böbreklerin ikisinin de etkilendiğini ve bunun DAMRG'da değişiklere yol açtığını göstermektedir.
Son dönem böbrek yetersizliğinin en sık nedeni olan diyabetik nefropatide asıl amaç diyabetes mellitus tanısıyla takip edilen hastalarda diyabetik nefropati gelişme ihtimali olan hastaların belirlenebilmesi ve erken dönemde diyabetik nefropatinin varlığının gösterilebilmesidir. Diyabetik hastalarda DN gelişimi açısından mikroalbuminüri ve üriner protein atılımının ölçülmesi riske sahip hastaların belirlenmesinde yardımcıdır. Ancak mikroalbuminüri seviyelerinin düşük olması glomerüler bozukluğun olmadığı anlamına gelmez. Tekrarlanan böbrek biyopsileri nefropatinin erken evrelerini belirlemek için kullanışlı bir yol değildir ve bazı histolojik değişiklikler DN'yi önceden haber vermediğinden yanlış yönlendirmelere neden olabilir. Renal fonksiyonlar genellikle güvenilir olarak kabul edilen nükleer tıp teknikleriyle değerlendirilebilir ancak bu yöntem iyonizan radyasyon içerir ve çözünürlüğü düşüktür ve renal korteks ve medulla ayrımı yapılamaz. Bu teknikle glomerüler filtrasyon hızı ve efektif plazma renal akımı değerlendirilebilirken böbrek difüzyonu ve perfüzyonu değerlendirilemez.
Görünür difüzyon katsayısı değer ölçümleriyle birlikte difüzyon MRG bir fonksiyonel görüntüleme yöntemi olarak tanı ve ayırıcı tanıda önemli katkılar sağlayabilir. Kontrast madde kullanımına gerek olmaması, uygulamanın kolay olması ve görüntülerin saniyeler içinde elde edilebilmesi önemli avantajlardır. Dokudaki su difüzyonu değerlerinin ADC haritaları üzerinden direkt olarak ölçülüp matematiksel olarak ortaya konabilmesi diğer fonksiyonel görüntüleme yöntemlerine kıyasla büyük bir üstünlüktür. Diyabetes mellitus tanısıyla takip edilen hastalarda DAMRG ile çalışmamızda tespit ettiğimiz orta ve yüksek renal ADC değerlerindeki düşüşün saptanması, erken dönemde henüz mikroalbuminüri gelişmeden diyabetik nefropatinin araştırılmasında yardımcı olabilir veya bu tür olguların daha yakından takip edilmesinde yol gösterici olabilir. Ancak DAMRG'nin diyabetik nefropatideki olası rolünün ortaya konulabilmesi için geniş serilerle yapılmış ve standardize edilmiş böbrek ADC değerlerine ihtiyaç vardır.
Sonuç olarak; iyonizan radyasyon içermeyen ve hızlı bir yöntem olan renal difüzyon ağırlıklı MR görüntüleme, önümüzdeki yıllarda diyabetik olgulardaki renal hasarı erken dönemde belirlemede ve evrelemede yardımcı bir yöntem olabilir.