Amerika Birleşik Devletleri'nde 2008 yılında kansere yakalanan kadın sayısının yaklaşık 700.000 olduğu tahmin edilmektedir
11. Ülkemizde de kanser hastalıklarının çok önemli bir sağlık sorunu olduğuna şüphe yoktur. İkibin altı yılında toplanan Sağlık Bakanlığı Epidemiyoloji ve Kanser Kayıt Alt Danışma Kurulunda aktif kanser kayıtsistemi 14 ilden 8 ilin kanser verilerinin yayınlanmasına karar verilmiştir. Bu iller Ankara, Antalya, Samsun, Erzurum, Trabzon, İzmir, Edirne ve Eskişehir'dir. 2005 yılında Türkiye nüfusu 72 milyon 65 bin olarak belirlenmiştir. Bu 8 ilin toplam nüfusu 14.273.465 olarak hesaplanmış olup toplam nüfusun yaklaşık %20 sini temsil etmektedirler
12. Bu oran sağlıklı bir istatistik vermek için yeterli gibi görülmektedir. Buna göre 1999-2005 yılları arasında kanser insidansı yaklaşık 100 binde 58 den 100 binde 173'e çıkmıştır. Kadınlarda en fazla görülen 5 kanser türü sırasıyla (yüzbinde) meme (35.4), deri (17.8), tiroid (8.4), akciğer ve bronş (7.2), ve mide (2.91.)'dir
12. Yıllar içinde tüm illerden bilgi akışı sağlandıkça daha sağlıklı ve güncel kanser verilerine ulaşılacaktır. Yeni kombinasyon kemoterapileri ve radyoterapi rejimlerinin üreme sistemi üzerine önemli olumsuz etkileri olduğu bilinmektedir
4,6. Bu negatif etkinin boyutu tedavinin sitotoksik potansiyeli, dozu, süresi ve hastanın yaşına bağlı olarakdeğişebilmektedir
4-7. Prematür over yetmezliği dışında uzun dönemli olarak bu hastaların gebeliklerinde kötü obstetrik sonuçlar ortaya çıkabilmektedir
13. Bunlara örnek olarak preterm eylem, düşükler, düşük ve çok düşük ağırlıklı bebek doğumları sayılabilir
13. Ovaryan rezerv primordiyal folliküllerin sayısı tarafından belirlenir. Özellikle primordiyal follikülleri hedefleyen herhangi bir toksik etki reproduktif yaşam aralığını kısaltabilir
4-7. Bunun yanı sıra prematür over yetmezliği oluşumunu indükleme riski de daha yüksektir. Prematür ovaryan yetmezliğin altında, mekanizma olarak germ hücrelerinin prematür, kitlesel ve hızlı ölümü (apoptosis) yatar
6,7. Oositi çevreleyen steroid üreten somatik hücre katmanlarına (granüloza ve teka hücreleri) toksik etkide bunlara neden olabilir
14. Giderek artan bir ilgiyle, 40 yaş altı kadınlarda anti kanser tedavi sonrası fertilitenin korunması konusu çalışılmaktadır. Genç kanser hastalarının fertilitelerinin korunması konusunda Amerikan Klinik Onkoloji kurumu bir kılavuz yayınlamıştır. Başka kurumlar da bu konuda teşvik edici yayınlar yapmaktadır
15,16. Esas olarak kanser kemoterapilerinin amacı hücre ölümünü apoptozis yolu ile uyarmaktır. Bu etki tüm vücutta olduğu gibi overde de apoptozisin uyarılması şeklindedir
17.
Kemoterapi ve radyoterapinin over dokusu üzerindeki uzun dönem etkisi, infertiliteye neden olan azalmış ovaryan rezerv ve prematür ovaryan yetmezliktir. Ovaryan rezervin göstergesi primordial follikül sayısıdır17,18. Kemoterapi ile indüklenmiş ovaryan hasarın ultrastrüktürel göstergesi yaygın follikül kaybı ve ovaryan fibrozistir19. Bununla birlikte kanser tedavilerinin ovaryan stromal hücrelere etkisi de önemlidir17-19. Ovaryan stromal hücreler endokrin fonksiyon görür ve büyük olasılıkla kemoterapi sonrası hasarın tamirinde rol oynar18-20. Kemoterapi sonrası ovaryan yetmezliğe etki eden faktörler arasında hasta yaşı, kemoterapi ajanının türü, ilacın kümülatif dozu ve kemoterapi öncesi ovaryan rezerv durumu sayılabilir. Yaşlı hastalarda ovaryan yetmezlik gelişmesi, aynı doz kemoterapi alan genç hastalara göre daha olasıdır. Örneğin ovaryan yetmezliğe sebep olacak kümülatif siklofosfamid dozu 40'lı yaşlardaki bir hasta için 5.2 g iken 30'lu yaşlarda 9.3 g, 20'li yaşlarda 20.4 g olmaktadır4,19.
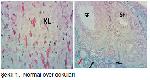
Alkilleyici ajanlar en yüksek follikül kaybına sebep olmaktadır4,5. Hücre siklusuna spesifik değillerdir yani hücre bölünme sırasında olmasalar da tek sarmal yada çift sarmal DNA kırıklarına neden olarak etki gösterirler11,18. Folliküler hasar yanında, DNA cross-link oluşturarak, steroid sentezinin azalmasıyla karakterize yaygın granüloza hücre hasarına da neden olurlar4,5,11,18,21. Bu grubun üyesi olan N-mustardlardan olan Siklofosfamid birçok antikanser protokolde kullanılmaktadır2,18,21. Bu, her yıl birçok kadının siklofosfamid nedenli ovaryan yetmezliğe girdiği anlamına gelir. Kanser sağ kalım oranlarının arttığı düşünülürse bu kadınların fertilite koruyucu yöntemlere yöneleceği açıktır11,18. Bu yöntemlerden kriyoprezervasyon yöntemleri, ovaryan transpozisyon işlemleri bilinmektedir. Üzerinde çalışmalar yürütülen alternatiflerden birisi de apoptozis inhibitörleridir18. Bizde çalışmamızda Siklofosfamid verilen grupta follikül sayısındabelirgin derecede azalma ve dejenere olmuş follikülleri yaygın olarak izledik. Öktem ve ark.17, yaptıkları ovaryan xenograft modelinde; tek doz 200 mg/kg siklofosfamid uygulanması ile 72 saat içerisinde bütün primordiyal follikülerin %97'sinin kaybolduğunu ve follikül kaybının ilaç enjeksiyonunu takiben oniki saat gibi kısa bir süre zarfında başladığını göstermişlerdir. Bu çalışmayla uyumlu olacak şekilde, siklofosfamide verilen gurupta ilk yedi günde over rezervinin %80 etkilendiğini izledik.
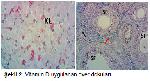
Doksorubisin, antrasiklin grubu antibiyotikler olarak sınıflandırılır. Antrasiklinlerin hücre tipine göre değişen etkileri vardır. Bu etkiler en belirgin siklusun S ve G2 fazlarında görülür6,7. Bu ilaçlar seçicilik göstermeksizin birbirine yakın baz çiftleri arasına girerek DNA ve RNA sentezini engellerler7. Doksorubisin, en önemli ve en sık kullanılan kemoterapötik ilaçlardan birisidir. Sarkomların, meme ve akciğer kanserleride dahil olmak üzere karsinomların, akut lenfosittik lösemilerin ve lenfomaların tedavisinde kullanılmaktadır22. Doksorubisinin over rezervine olumsuz etkileri mevcuttur5,6. Bu çalışmada doksorubisin verilen grupta folliküllerde sayıca azalma ve dejenere follikülleri yaygın olarak izlendi ve bunlarda tunnel metodu ile apopitozisin yaygın olduğunu görüldü.
Kanser tedavisine bağlı olarak ortaya çıkan over yetmezliği hastayı hem menopoz, hem de infertilite riski ile karsı karsıya bırakmaktadır23,24. Bu hastalar kemoradyoterapi ile sterilize olmasalar bile, erken gebelik kayıpları, prematür eylem ve düşük doğum ağırlığı riski ile karsı karsıya kalmaktadırlar23. Kanser tedavisi öncesinde ve sonrasında fertilitenin korunması için medikal ve cerrahi yöntemler mevcuttur. Fakat bunların tam koruyucu etkileri net değildir24-29.Uzun etkili gonadotropin analogları26,27 GnRH antagonistleri28, antioksidanlar29 over rezervini korumak amaçlı kullanılmaktadır26-29.
Kanserin önlenmesi ve bazı kanser tiplerinin tedavisinde (kolorektal, meme, prostat, over, mesane, akciğer, deri kanserleri ve lösemi) vitamin D bileşiklerinin önemli bir role sahip olduğu birçok epidemiyolojik ve klinik çalışmalarda gösterilmiştir8-10. Vitamin D hem anti-proliferatif etkiyle, hem de anjiyogenezi inhibe ederek hücrelerin apoptozisini engeller9,10. Vitamin D aynı zamanda tümörün yayılımını kolaylaştıran telomeraz ekspresyonunu, apoptozisi ve anjiyogenezi inhibe etmektedir30-32. Ayrıca vitamin D, DNA'yı tamir eden genlerle, genomun bütünlüğünü sağlayan genlerin ekspresyonunu uyarmaktadır32.
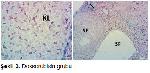
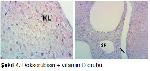
Ratlar üzerinde yapılan bir çalışmada hormon duyarlı meme kanseri tedavisinde Vitamin D'nin tümör ilerlemesini engellediği gösterilmiştir33. Ratlarda oluşturulan barsak tümörlerinin gelişiminin engellenmesinde de vitamin D'nin olumlu etkileri bildirilmiştir34. Bu çalışmada, doksorubisin ve siklofosfamid verilen grupta Vitamin D'nin over rezervini korumada olumlu etkisi görülmedi. Kılıç ve ark.35 siklofosfamid verilen ratlarda ovaryen toksitenin azaltılmasında kemik iliğinden alınan mezenkimal kök hücrelerin olumlu etkisini göstermişlerdir. Bu olumlu etkileri, özelikle DNA hasarının engellenmesi ve apopitozisin azaltılmasına bağlamışlardır. Gürgen ve ark.36 siklofosfamid verilen ratlarda selenyumun ovaryen toksitenin azaltılmasında olumlu etkisini göstermişlerdir. Wietrzyk ve ark.37 farelerde verilen yeni vitamin D analoglarının sitoksik etkileri önleyemediğini saptamışlardır.
Kanser hastalarında, fertilitenin korunmasında apoptozis inhibitörleri, etkili olabileceği düşünülen, ancak deneysel ve klinik bilginin henüz yeterli olmadığı bir konudur. Bu çalışmada, Vitamin D ek doz uygulamasının, Siklofosfamid ve Doksorubisin'in sitotoksik etkisini önleyemediği görüldü.