TRP kanalları, çeşitli iç ve dış uyaranlar için hücresel sensörler olarak işlev gören kanallardır
5. Tanımlanmış 28 memeli TRP kanalı izoformu olup bunlardan en az 19'u (TRPC'nin tümü, TRPV1, TRPV2, TRPVV4, TRPP1, TRPP2ler ve TRPMM5 hariç tüm TRPM'ler) vasküler endotelyal hücrelerden eksprese edilir
6,7. Bu kanallar arasında, TRPC1, -C4, -C6 ve -M7, endotelyal bariyer disfonksiyonu ve bozulmuş anjiyojenik süreçlerle bağlantılıdır
8. TRPC3, -C4, -M2 ve -M7 oksidatif hasar ve hücre ölümünden sorumlu izotiplerdir
7,9.
TRPM2 ve TRPM7 kanalları başta beyin ve kemik iliği olmak üzere böbrek, bağırsak, karaciğer, akciğer, testis gibi pek çok dokuda tespit edilmiştir. TRPM2 ve TRPM7 kanalları ya direkt olarak plazma zarındaki Ca+2 giriş kanalları gibi davranarak ya da sitozolik serbest Ca+2 kanallarında değişime yardımcı olarak etkilerini gösterirler. Metabolizma sonucu üretilen serbest oksijen radikalleri TRPM2 ve TRPM7 kanallarını aktive eder. Bu kanalların aktivasyonu hücre içi Ca+2 iyonu artışına, bu da hücre ölümüne kadar varabilen çeşitli patofizyolojik olayların başlamasına sebep olmaktadır 10,11. Günümüz dünyasında en önemli sağlık sorunlarından biri olarak kabul edilen diyabetes mellitus (DM), kardiyovaskuler, serebrovasküler ve nefrotik komplikasyonları ile mortalite ve morbiditeye neden olmaktadır. DMün karaciğerde hepatosit hasarı, inflamasyon ve fibrozis ile ilişkisi bilinmekte olup bu değişikliklere, hipergliseminin neden olduğu oksidatif stres aracılık etmektedir 12,13. Hepatosit hasarı, hepatik yıldız hücrelerini aktive etmekten sorumlu tutulan Kupffer hücrelerinden inflamatuar sitokinlerin salınmasını indükler. Fibrozis, doku hasarına yanıt olarak gelişir ve esas olarak hepatik stellat hücreler tarafından salgılanan ekstraselüler matriks birikimine neden olur 14. Karaciğer fibrozisi karmaşık bir patolojik süreçtir. Çeşitli patolojilerin neden olduğu yaralar tekrar tekrar iyileşir, yara izleri oluşturur ve sonunda karaciğer fibrozisine dönüşür. Karaciğer fibrozisi kontrol altına alınmazsa, karaciğer sirozuna ve hatta karaciğer kanserine yol açabilir. Uygun tedaviler karaciğer fibrozis sürecini yavaşlatabilir. Bu nedenle, karaciğer fibrozunun etkili tedavisi son derece önemlidir ve karaciğer fibrozisi için yeni terapötik hedefler bulmak acildir 15. Hepatik stellat hücrelerin aktivasyonu ve proliferasyonunun, hepatik fibroz oluşumu ile ilişkili olduğu düşünülmektedir. Bu nedenle, hepatik stellat hücrelerin aktivasyonunu ve proliferasyonunu inhibe etmek, karaciğer fibrozisini hafifletmede önemli bir adımdır. Karaciğer hasarına neden olan önemli bir faktör, dinlenme durumundaki hepatik stellat hücrelerinin aktive edilmiş miyofibroblastlara dönüştürülmesidir. Sonrasında gelişen kolajen birikimi, belirgin yara izlerine yol açar 16. Bu sebeple, hepatik yıldız hücrelerinin aktivasyonunu veya proliferasyonunu inhibe etmek ve ekstraselüler matriks oluşumunu bloke etmek, terapötik müdahale için anahtar stratejilerdir 17. Bununla birlikte, fibrogenezi yönlendiren moleküler mekanizmalar hala tam olarak anlaşılamamıştır. Şu anda birkaç anti-fibrotik terapötik strateji, etkili olmasına rağmen gelecekte karaciğer hasarının tedavisi için etkili hedefler bulmak hala güncel bir konudur. TRPM2, TRPM7 iyon kanalları sayısız hastalık modelinde karşımıza çıkan etkili moleküllerdir 18-20.
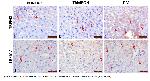
Bizim çalışma bulgularımız diyabetik sıçan karaciğer dokularında TRPM2 ve TRPM7 ekspresyonunun arttığını gösterdi. Bu durum litaretür bilgileriyle örtüşmekte olup diyabete bağlı karaciğer patolojilerine yönelik bir bulgu olabilir. TRPM2, hücre ölümü, sitokin üretimi, oksidatif stres ve hatta fibrozis dahil olmak üzere çeşitli fizyopatolojik süreçlerde yer almaktadır. Örneğin, oksidatif stresin neden olduğu hücre ölümünde TRPM2 kanallarının aktivasyonu önemli bir faktördür 21. Önceki bir çalışmada yazarlar TRPM2 ekspresyonunun, sıçan kardiyak fibroblastlarında hipoksi tarafından indüklenen, insan fibroblastlarında tip I kollajene benzer şekilde bir birikime neden olarak, kardiyak fibrozise katkı sağladığını gösterdiler 22. TRPM2 inhibisyonunun, oksidatif stres, inflamasyon ve apoptozu hafifleterek iskemik akut böbrek hasarını önlemede etkili olduğu ve inflamatuar yanıtı inhibe ederek, iskemi/reperfüzyona bağlı akut böbrek hasarını iyileştirdiğini gösterdi 23. TRPM 7 ise iyon kanalı ve kinaz olarak ikili işlevleri olan bir zar proteinidir. Ca+2 ve Mg+2 iyonlarının akışını düzenleyerek çeşitli hücrelerin aktivasyonuna ve çoğalmasına katkı sağlamaktadır 24. TRPM7 kanalları; hücre çoğalması, hayatta kalma, farklılaşma, göç, yapışma, embriyonik gelişim ve nörotransmiter salınımı gibi çeşitli fizyolojik süreçlere de aracılık etmektedir 25. TRPM7'nin inflamatuar böbrek hasarı sırasında arttığı ve TRPM7 ekspresyonunun inhibe edilmesinin, progresif renal fibrozise karşı koruma sağladığı gösterilen tek taraflı üreter obstrüksiyonu böbreğinde, renal atrofiyi önleyebileceği gösterildi 26,27. Oksidatif stres kaynaklı hücre hasarında önemli bir role sahip olup TRPM7 ekspresyonunun baskılanmasının, Ca+2 alımını azaltarak nöronal sağkalımı artırdığı bilinmektedir. TRPM7'nin hücre ölümüne aracılık etme yeteneğinde birden fazla iyon iletiminin rol oynadığı fikriyle tutarlı olarak, insan embriyonik böbrek hücrelerinde TRPM7'nin aşırı ekspresyonu, ROS üretiminin artmasına neden olan Mg+2 ve Ca+2 akışını artırmaktadır 28. Son zamanlarda, TRPM7 ekspresyonunun, H2O2 tarafından artırıldığı ve TRPM7in oksidatif stresin bir belirteci olabileceği düşünülmekte olup yapılan çalışmalarda CCl4 ile indüklenen karaciğer fibrozisinde farelerin karaciğerlerinde TRPM7 ekspresyonunun arttığı gösterilmiş ve TRPM7 için spesifik bir inhibitör kullanılarak anti-tümör, anti-inflamatuar ve anti-hepatik fibroz aktiviteler elde edilebileceği belirtilmiştir 29-31.
Çalışmamız TRPM2 ve TRPM7 ekspresyonunun diyabetik karaciğer dokularında arttığını gösterdi. Bu bulgu TRPM2 ve TRPM7 nin patolojik süreçlerdeki katkısı düşünüldüğünde, diyabete bağlı karaciğer patolojilerini de açıklayabilir ve TRPM2 ve TRPM7 üzerinde bloke edici etkili farmakolojik ajanların karaciğer fibrozisinin tedavisini amaçlayan ileri çalışmalara ışık tutabilir
Sonuç olarak; TRPM2 ve TRPM7'nin karaciğer fibrozisinin tedavisi için bir ilaç hedefi olabileceğini düşünmekteyiz. Bu nedenle, etkili bir TRPM2 ve TRPM7 inhibitörü arayışı, karaciğer fibrozisinin tedavisinde yeni bir yöntem gibi görünmektedir.