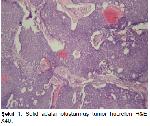
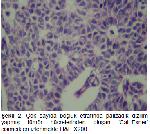
Granüloza hücreli tümörler düşük malign potansiyeli
olan over tümörleridir. Bu nedenle fertilitesini korumak
isteyen ve evre 1A döneminde tanı konulan genç
hastalarda unilateral salpingo-ooferektomi yeterli olurken,
postmenopozal dönemdeki hastalara genel olarak total
abdominal histerektomi ve bilateral salpingo-ooferektomi
uygulanır. Konservatif tedavi uygulanan hastalarda tümör
dokusundan salgılanan östrojene bağlı olarak
endometriumda gelişebilecek endometrial karsinoma
karşı dikkatli olunmalı gerekli durumlarda endometrial
biopsi ile endometrial karsinom ekarte edilmelidir. Yine
konservatif tedavi uygulanan hastalarda (unilateral
salpingo-ooferektomi) tümörün %2 gibi bir oranda
bilateral olabileceği göz ardı edilmemelidir.
GHT'lerin preoperatif dönemde epitelyal over
tümörlerinden ayırt edilmesinin zor olması ve
intraoperatif dönemdeki patolojik tanısının net
konamaması nedeniyle operasyon sırasında diğer over
tümörlerinde olduğu gibi laparatomi sırasında evreleme,
total abdominal histerektomi, bilateral salpingoooferektomi
ve omentektomi de başlangıç tedavisi olarak
seçilebilir (10).
Genellikle operasyon sonrası kemoterapi yüksek risk
faktörlü hastalarda (tümörde rüptürün olması, evre 1C ve
daha ileri evrede olması, tümör çapının 10 cm'den daha
fazla olması) ya da nüks izlenen hastalarda önerilir.
Yapılan çalışmalarda PVB (cisplatin + vinblastin +
bleomycin) ve BEP (bleomycin + etoposide + cisplatin)
rejimlerinin etkili olduğu gösterilmiştir11,12.
Yeni yapılan çalışmalarda gonodotropin releasing
hormon agonistleri ve aromataz inhibitörleri gibi ilaçların
da tedavide etkili olduğu gösterilmiştir13,14.
Granüloza hücreli tümörlerin hormon aktif tümörler
olması nedeniyle operasyon sonrasındaki dönemlerde
farklı tümör belirteçleri takipte kullanılabilir. Östrodiol,
antimüllerian faktör (AMH), inhibin A, inhibin B ve follikül
stimüle edici hormon (FSH) serum tümör belirteci olarak
kullanılabilmesine rağmen bu belirteçlerin hiç birisi
tümöre spesifik değillerdir2,3.
GHT'li olgularda serum östrodiol seviyesindeki
yükseklik dikkat çekici olmasına rağmen, %30 olguda
hastalığın progresyonunda artış izlenmemiştir. Bu
nedenle hastalığın aktivitesini göstermede güvenilir bir
belirteç değildir.
Üreme çağındaki kadınlarda gelişen folliküllerdeki
granüloza hücrelerinden salgılanan AMH menopoz
sonrasındaki dönemde normalde kanda saptanmazken,
GHT'li olan kadınlarda progresif olarak düzeyinin
yükseldiği ve remisyonda saptanmadığı görülmüştür15. Bu nedenle tümöre en spesifik serum belirteçi
olarak kabul edilir.
İnhibin, normal over folliküllerindeki granüloza
hücrelerinden salgılanır ve negatif feedback etki ile
hipofizden salgılanan FSH' ın regülasyonunda rol oynar.
İnhibin alfa ve beta olmak üzere iki subünitten oluşur.
Postmenopozal dönemde 1-3. yıllarda FSH' da 10-20 kat
artış olmakta, sonraki yıllarda ise FSH seviyeleri yavaş
yavaş düşmektedir. İnhibin salınımında da 35 yaşlarından sonra bir azalma başlamakta 40 yaşlarından
sonra bu azalma daha hızlı olmaktadır. Premenopozal
ve postmenopozal dönemlerindeki artmış inhibin ve
azalmış FSH düzeyleri uyarıcı olabilir fakat spesifik
değildir. GHT' de her iki subünitte artış olmasına rağmen
özelikle inhibin beta artar fakat inhibin yükseklikleri GHT
için spesifik değildir2,3.
Hastalığın prognozunda en önemli faktör
evrelemedir. Evre 1 ve 2 de bulunan hastaların 5 yıllık
yaşam oranları %95'e ulaşırken, evre 3 ve 4 deki
hastalarda bu oran %59' lardadır16.
Evreleme epitelyal over tümörlerinde kullanılan
sisteme uygun yapılmaktadır. Büyük tümör boyutu ve
tümörde rüptür olması, tümörde artmış mitotik indeks,
lenfovasküler alan invazyonu kötü prognoz ile ilişkili
bulunmuştur.
GHT düşük gradeli malignitelerdir ve uzun dönem
takip gerektirirler. Ortalama rekürrens zamanı ilk tanıdan
yaklaşık 4-6 yıl sonradır. Bu nedenle hastalar düzenli
klinik takiplere alınmalı ve serum tümör belirteçleri
izlenmelidir.
Sonuç olarak premenopozal ve postmenopozal
dönemde kanama şikayeti bulunan hastalar dikkatlice
yapılan fizik muayene ve transvaginal ultrason
sonrasında mutlaka endometrial biopsi ile
değerlendirilmelidir. Endometrial hiperplazi gibi artmış
östrojen aktivitesini düşündüren durumlarda overin
hormon aktif olan tümörü olan granulosa hücreli tümörleri
akıldan çıkarılmamalıdır.